Nun wissen wir also, dass bei einer RedOx-Reaktion immer ein Elektronenübergang stattfindet. Dabei wird ein Reaktionsteilnehmer reduziert und ein anderer oxidiert. Woran können wir aber nun erkennen, ob es sich um eine RedOx-Reaktion handelt? Dazu betrachten wir die Oxidationszahl der Reaktionsteilnehmer, die in manchen Büchern auch Oxidationsstufe genannt wird.
Aber was ist eine Oxidationszahl?
Bei der Oxidationszahl handelt es sich um eine Angabe zur Elektronendichte eines Atoms, oder Moleküls. Diese Elektronendichte und somit auch die Oxidationszahl ändert sich für jeden Reaktionsteilnehmer im Verlaufe einer RedOx-Reaktion.
Je höher die Elektronendichte, desto mehr negative Ladungen sind vorhanden. Dementsprechend ist die Oxidationszahl niedriger.
Je niedriger die Elektronendichte, desto weniger negative Ladungen sind vorhanden.
Dementsprechend ist die Oxidationszahl höher.
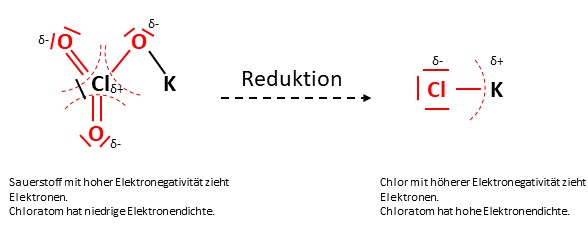
Bei einer Reduktion wird die Elektronendichte erhöht, wodurch die Oxidationszahl geringer wird.
Elemente mit hoher Elektronegativität ziehen Bindungselektronen eher an als Elemente mit niedriger Elektronegativität.
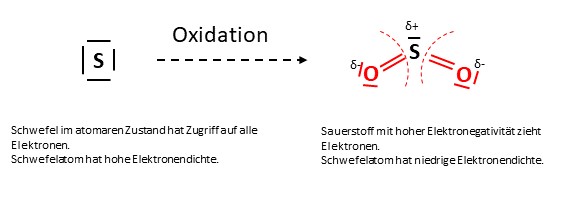
Bei der Oxidation wird die Elektronendichte geringer, weshalb die Oxidationszahl steigt.
Eine RedOx-Reaktion ist also jede Reaktion, bei welcher sich die Oxidationszahl der Reaktionsteilnehmer verändert. Bei unserer RedOx-Reaktion aus dem Feuerwerk würde das dann wie folgt aussehen.
Die Oxidationszahl gibt man übrigens immer in Römischen Zahlen oberhalb des jeweiligen Stoffs an.
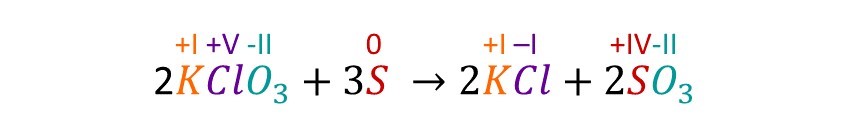
Bei der Veränderung der Oxidationszahl wird immer nur eines der Atome betrachtet, auch wenn es sich insgesamt um ein Molekül handelt. Deswegen wird hier nur die Veränderung des Chlor- und des Schwefelatoms betrachtet.
Nun wissen wir, was Oxidationszahlen sind, im nächsten Schritt lernen wir wie man diese bestimmen kann.
