Unter dem photoelektrischen Effekt oder kurz Photoeffekt versteht man die Wechselwirkung elektromagnetischer Strahlung (z. B. sichtbares Licht, Infrarot- und UV-Strahlung) und Materie. Beobachtet wurde dieser Effekt erstmals von Heinrich Hertz 1886, erklären konnte ihn jedoch erst Albert Einstein 1905. Mit seiner Erklärung wurde ein wichtiger Grundstein für die Quantenmechanik gelegt.
Der Begriff Photoeffekt bezeichnet hierbei mehrere, sich ähnliche Phänomene. Man unterscheidet unter anderem den äußeren und den inneren Photoeffekt.
Äußerer Photoeffekt
In diesem Fall treten Elektronen unter dem Einfluss elektromagnetischer Strahlung aus Metalle oder Halbleitern aus. Sie besitzen nach ihrem Austritt eine Geschwindigkeit und damit eine kinetische Energie.
Experimentelle Entdeckung
Aufbau
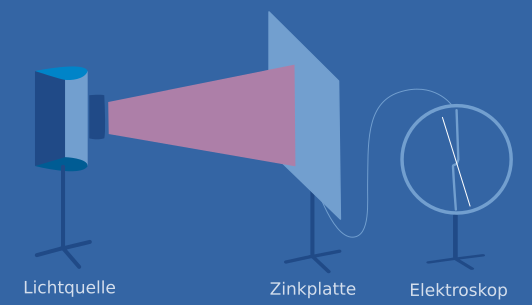
Eine Zinkplatte, die sowohl positiv als auch negativ geladen werden kann, ist mit einem Elektroskop verbunden. An diesem kann die momentane Ladung der Platte abgelesen werden.
Durchführung | Beobachtungen |
|---|---|
Experiment 1 | |
Platte positiv geladen | kein Effekt |
mit Rotlichtlampe bestrahlt | Ladung der Platte bleibt erhalten |
Experiment 2 | |
Platte positiv geladen | kein Effekt |
mit Hg-Lampe (Quecksilberdampf-Lampe) bestrahlt | Ladung der Platte bleibt erhalten |
Experiment 3 | |
Platte negativ geladen | kein Effekt |
mit Rotlichtlampe bestrahlt | Ladung der Platte bleibt erhalten |
Experiment 4 | |
Platte negativ geladen | Platte entlädt sich |
mit Hg-Lampe bestrahlt | Entladung setzt sofort ein, stoppt sobald Lichtquelle entfernt wird |
Experiment 5 | |
Platte negativ geladen | kein Effekt |
mit Hg-Lampe bestrahlt | Ladung der Platte bleibt erhalten |
Glasscheibe wird zwischen Lampe und Platte gebracht |
Folgerungen
Die Auslösung von Elektronen ist abhängig von der Wellenlänge und erfolgt instantan (ohne zeitliche Verzögerung).
Die Platte entlädt sich nur, wenn sie zuvor negativ geladen war (also ein Elektronenüberschuss herrschte). Somit können anscheinend lediglich negative Ladungsträger, also Elektronen, austreten. Eine Hg-Lampe strahlt Licht verschiedener Wellenlängen, aus u. a. im Bereich von grünem, blauen und UV-Licht. Rotes Licht besitzt eine andere Wellenlänge als Licht einer anderen Farbe und UV-Licht, Glas absorbiert UV-Licht. Daraus lässt sich schließen, dass der UV-Anteil der Hg-Lampe den Austritt der Elektronen hervorruft, nicht aber Licht der anderen Wellenlängen.
Dieses Experiment mit der Zinkplatte bildet jedoch erst den Anfang. Mit der Zeit wurden weitere Experimente entworfen und durchgeführt, um den Photoeffekt näher zu untersuchen.
Photozelle
Aufbau
Die Photozelle besteht aus einer Metallkathode und einer gegenüberliegenden Anode (meist in Form eines Drahtringes oder -gitters). Die Kathode wird dann mit Licht gewünschter Wellenlänge bestrahlt. Kommt es zum äußeren Photoeffekt, so treten Elektronen aus der Kathode aus und gelangen mit zur Anode. Dies ist in Form des sogenannten Photostromes messbar. Zudem lädt sich die Anode negativ und die Kathode positiv auf. Es wird somit ebenfalls eine Spannung erzeugt.
Gegenfeldmethode
Ein Ziel des Experimentes ist es festzustellen, welche Geschwindigkeit die Elektronen nach ihrem Austritt besitzen. Legt man an die Photozelle eine äußere Spannung an, die gegen die Bewegung der Elektronen von Kathode zu Anode gerichtet ist (also Kathode als Pluspol, Anode als Minuspol), so müssen die Elektronen das entstandene elektrische Feld überwinden. Sie besitzen jedoch nur eine bestimmte Geschwindigkeit und damit kinetische Energie. Ist die Spannung hoch genug, dann reicht diese Energie der Elektronen nicht mehr aus, um die Strecke von Kathode zu Anode zu überwinden und es ist kein Photostrom mehr messbar. Genau diesen Fall, dass der Photostrom Null ist, stellt man bei dem Experiment ein und kann aus der dann eingestellten Spannung folgendermaßen die kinetische Energie und Geschwindigkeit berechnen.
Energie des homogenen elektrischen Feldes
Kinetische Energie des Elektrons
Diese Energien müssen gleich groß sein. Man erhält somit:
Nun ist man in der Lage, mithilfe der Gegenfeldmethode die Geschwindigkeit der Elektronen nach ihrem Austritt zu bestimmen. Auch ohne konkrete Werte auszurechnen, kann man feststellen, dass je größer die angelegte Spannung ist, desto größer ist die Geschwindigkeit der Elektronen.
Durchführung | Beobachtungen |
|---|---|
Photozelle mit Licht gleicher Intensität aber verschiedener Wellenlänge (z.B. rotem, gelbem, grünem, blauem und violettem Licht) bestrahlt | erst ab bestimmter Farbe des Lichtes ist Photostrom messbar (z. B. bei rotem und gelbem Licht ist nicht messbar, sondern erst ab grünem Licht) |
Photostrom wird gemessen | mit sinkender Wellenlänge nimmt Photostrom zu |
eingestellte Spannung der Gegenfeldmethode wird gemessen | eingestellte Spannung nimmt ebenfalls mit kleiner werdender Wellenlänge zu |
Folgerungen
Die kinetische Energie der Elektronen ist abhängig von der Wellenlänge und antiproportional zu dieser, d.h. die Energie ist größer, je kleiner die Wellenlänge ist.
Führt man dieses Experiment mit verschiedenen Metallen als Kathode durch, stellt man außerdem fest, dass die größte Wellenlänge, bei der man noch einen Photostrom messen kann, von Metall zu Metall variiert. Dementsprechend unterscheiden sich auch die konkreten Geschwindigkeiten bei gleicher Wellenlänge. Es existiert folglich ein materialabhängiger Faktor.
Als letztes Experiment wurden die Zusammenhänge der Intensität der Strahlung und der Größe des Photostromes und der Spannung bei der Gegenfeldmethode untersucht. Der Aufbau des zweiten Experimentes bleibt dabei erhalten.
Durchführung | Beobachtungen |
|---|---|
Photozelle weiterhin mit rotem, gelbem, grünem, blauem und violettem Licht bestrahlt | Photostrom nimmt mit steigender Intensität zu |
Intensität der Strahlung wird variiert | eingestellte Spannung bleibt für die einzelnen Wellenlängen auch bei zunehmender Intensität gleich |
Folgerungen
Eine höhere Intensität führt dazu, dass in einer Zeiteinheit mehr Elektronen ausgelöst werden, nicht jedoch dazu, dass die ausgelösten Elektronen schneller sind.
Licht als klassische Welle
Der Photoeffekt konnte nicht grundlos einige Zeit lang nicht erklärt werden. Denn die Beobachtungen und Folgerungen widersprachen der damaligen Vorstellung des Lichtes als Welle. Eine Welle besitzt Energie, die abhängig von ihrer Amplitude (Intensität) ist. Trifft die Welle auf Materie, so nimmt die Materie kontinuierlich die Energie der Welle auf. Die Wellenlänge entscheidet lediglich darüber, wie schnell die Energie aufgenommen wird (kleine Wellenlänge heißt hohe Frequenz heißt schnellere Energieabgabe, große Wellenlänge heißt geringe Frequenz heißt langsamere Energieabgabe), nicht aber wie viel Energie die Materie aufnehmen kann.
Beobachtungen | Vorstellung |
|---|---|
Photoeffekt ist instantan | die aufgenommene Energie nimmt mit der Zeit zu, die Auslösung kann nicht für verschiedene Intensitäten sofort einsetzen, da das Licht erst lange genug einstrahlen müsste, um den nötigen Energiebetrag zu erreichen |
Photoeffekt ist wellenlängenabhängig | Wellenlänge sollte nur die Zeit ändern, die zum Austritt nötig ist, nach gewisser Zeit wollten für jede Wellenlänge Elektronen austreten |
Energie der Elektronen unabhängig von der Intensität immer gleich für eine Wellenlänge | bei höherer Intensität können die Elektronen in gleicher Zeit mehr Energie aufnehmen und sollten somit nach ihrem Austritt schneller sein als bei gleicher Wellenlänge aber niedrigerer Intensität |
Erklärung
Die Begründung des Photoeffektes konnte, wie wir gesehen haben, nicht durch die klassische Vorstellung des Lichtes als Welle geliefert werden. Licht muss somit nach einem anderen Modell beschrieben werden. Dieses Modell sind die sogenannten Lichtquanten. D. h. das Licht besteht aus kleinen Energiepakten. Diese Lichtquanten enthalten die Energie des Lichtes und sind zählbar, bewegen sich ohne sich zu teilen und können nur als Ganzes absorbiert werden. Zudem ist die Energie des Quants abhängig von der Wellenlänge und alle Lichtquanten der gleichen Wellenlänge besitzen die gleiche Energie. Ein Elektron kann somit nicht kontinuierlich jeden möglichen Energiebetrag aufnehmen, sondern lediglich ein Lichtquant absorbieren und dessen gesamte Energie aufnehmen oder kein Lichtquant aufnehmen und damit auch keine Energie. Später wurde die Bezeichnung Lichtquant durch den Begriff des Photons ersetzt. Licht bestand nun aus unteilbaren, zählbaren Teilchen.
Was geschieht nun in einem Metall?
Die Elektronen in dem Metall absorbieren die Photonen der eintreffenden Strahlung, wobei ein Elektron genau ein Photon absorbiert. Dabei gibt das Photon seine gesamte Energie an das Elektron ab und existiert danach nicht mehr. Das Elektron besitzt nun eine höhere Energie als zuvor. Ist diese Energie groß genug, kann das Elektron aus dem Atomverbund des Metalls austreten. Die Energie, die zur Auslösung (Emission) der Elektronen nötig ist, hängt von dem bestrahlten Material ab und wird Austrittsarbeit genannt. Diese Austrittsarbeit muss in jedem Fall überwunden werden. Da der Austritt nur noch bei einer maximalen Wellenlänge vonstattengeht, muss bei noch größeren Wellenlängen die Energie der Photonen kleiner sein als die nötige Austrittsarbeit. Ist die Wellenlänge geringer (d. h. die Frequenz höher), so besitzen die Elektronen nach dem Austritt eine kinetische Energie, die sich folgend berechnen lässt:
Wobei die Austrittsarbeit und das Plancksche Wirkungsquantum (eine Naturkonstante) darstellt.
beschreibt somit den Zusammenhang von Frequenz und der Energie eines Photons.
Ändert man die Intensität des Lichtes, absorbiert ein Elektron weiterhin nur ein Photon und nimmt somit dieselbe Energie wie vorher auf. Einzig die Anzahl der emittierten Elektronen, nicht jedoch deren Energie verändert sich. Bei höherer Intensität werden mehr Elektronen pro Zeiteinheit emittiert, was zu einem höheren Photostrom führt.
Grundsteinlegung der Quantenmechanik
Der Photoeffekt bzw. seine Erklärung führte dazu, dass das bis dahin genutzte Modell für Licht als Welle nicht mehr richtig war. Man konnte jedoch auch nicht vernachlässigen, dass viele Phänomene des Lichtes mithilfe des Wellenmodells erklärbar waren. Dies führte im Endeffekt dazu, das Licht sowohl als Welle als auch als Teilchen anzusehen. Dieser sogenannten Wellen-Teilchen-Dualimus ist ein wichtiges Prinzip der Quantenmechanik.
Innerer Photoeffekt
Im Gegensatz zum äußeren Photoeffekt tritt der innere bei Halbleiter auf und es treten keine Elektronen aus dem Material aus. Viel mehr führt die Absorption der Photonen und die damit verbundene Erhöhung der Energie der Elektronen dazu, dass die Elektronen die bei Halbleitern vorhandene Energielücke überwinden. D. h. die Elektronen, die normalerweise an die Atome gebunden sind und sich im Valenzband befinden, können in das Leitungsband springen und sind quasi als freie Ladungsträger zu betrachten. Erst wenn in einem Material frei bewegliche Ladungsträger vorhanden sind, kann es zu einer elektrischen Leitfähig des Materials kommen. Der innere Photoeffekt ist somit für Leitungseigenschaften von Halbleitern verantwortlich.
Du hast noch nicht genug vom Thema?
Hier findest du noch weitere passende Inhalte zum Thema:
