Die Chiralität beschreibt eines der wichtigsten Prinzipien in der Natur. Sie bezeichnet die Tatsache, dass es Dinge gibt, die sich zueinander wie Bild und Spiegelbild verhalten, aber dennoch nie zur Deckung gebracht werden können.
Der Begriff Chiralität leitet sich aus dem Griechischen ab und wird häufig mit Händigkeit übersetzt.
Unsere Hände sind übrigens auch chiral, das kannst du ganz einfach sehen, wenn du beide Hände mit den Handflächen nach unten vor dich hältst. Dann kannst du sehen, dass sie wie Bild und Spiegelbild aussehen. Versuchst du nun sie übereinander zu legen, kannst du schnell sehen, dass sie nicht deckungsgleich sind.
Wenn du eine Hand umdrehst, kannst du deine Hände zwar aneinander legen, aber deckungsgleich sind sie trotzdem nicht, da du bei einer Hand nun deine Fingernägel sehen kannst und bei der anderen nicht.

Chiralität in der Chemie
Chirale Moleküle bestehen aus denselben Bestandteilen und unterscheiden sich nur in deren Anordnung. Trotzdem unterscheiden sich die Moleküle in ihren physiologischen und optischen Eigenschaften.
In der Chemie beschreibt Chiralität die besondere Stereochemie, beziehungsweise räumliche Anordnung von Atomen in einem Molekül. Ähnlich wie bei dem Beispiel mit den Händen, ähneln sich chirale Moleküle sehr, sie besitzen nämlich dieselbe Summenformel. Aber sie verhalten sich zueinander wie Bild und Spiegelbild und sind nicht deckungsgleich.
Die besondere Form der Stereoisomerie, welche chirale Moleküle hervorbringt, heißt Enantiomerie.
Ein Beispiel für ein chirales Molekül ist die Aminosäure Alanin, hier sind beide Isomere der Aminosäure abgebildet.
Chiralität kann nur im dreidimensionalen Raum dargestellt werden, weshalb die Darstellung im zweidimensionalen manchmal schwierig nachzuvollziehen ist.
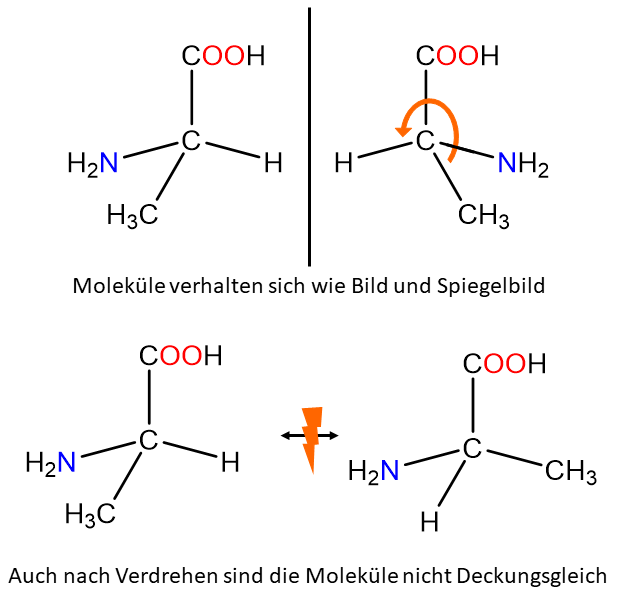
Hier abgebildet ist die Aminosäure Alanin, wie du sehen kannst, ist sie chiral, da alle oben genannten Eigenschaften zutreffen.
Nomenklatur chiraler Moleküle
Um chirale Moleküle eindeutig benennen zu können, wurde das R/S-System entwickelt. Dafür wird zuerst dem Substituenten mit der niedrigsten Priorität die Nummer 1 zugewiesen, dem nächsthöheren die 2 und so weiter.
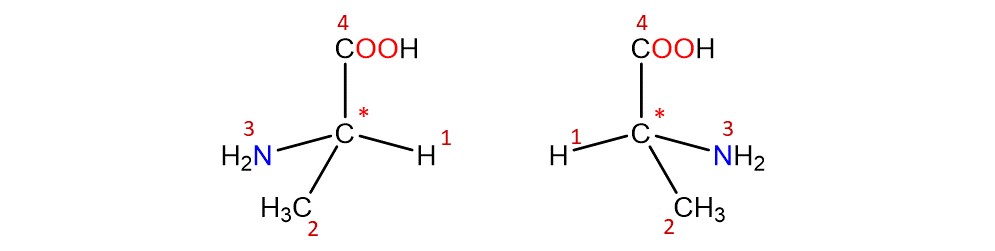
Im nächsten Schritt wird der Substituent mit der niedrigsten Priorität "nach hinten" gedreht, sodass er nicht mehr sichtbar ist. Nun kann man die restlichen Substituenten betrachten und sehen, ob die Priorität der Substituenten im Uhrzeigersinn, oder gegen den Uhrzeigersinn zunimmt.
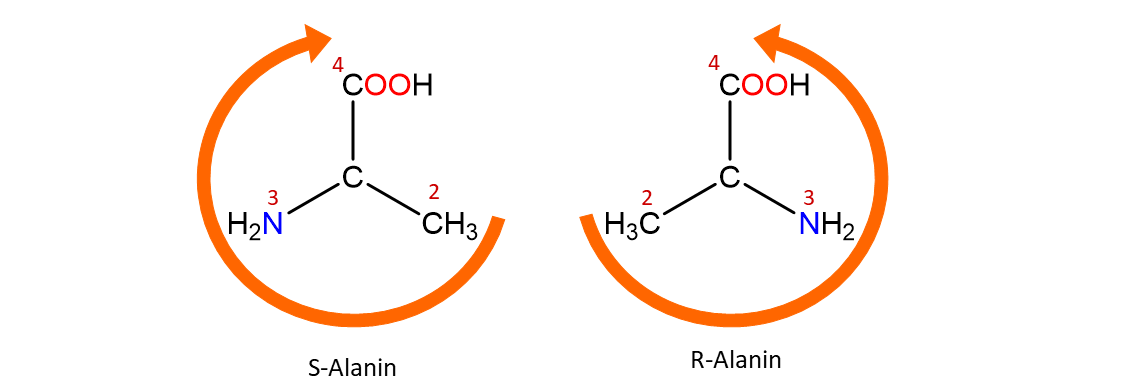
Nimmt die Priorität im Uhrzeigersinn zu (Linksdrehend) erhält die Verbindung den Suffix S-. Nimmt die Priorität im Uhrzeigersinn ab (Rechtsdrehend) erhält die Verbindung den Suffix R-.
Diese Drehung kann mithilfe eines Polarimeters gemessen werden.
Eigenschaften
Chirale Moleküle unterscheiden sich nicht in ihren chemischen Eigenschaften und nur in einer physikalischen, dem spezifischen Drehwinkel. Mehr dazu kannst du im Artikel zur Optischen Aktivität erfahren.
Neben dem spezifischen Drehwinkel unterscheiden sich manche chiralen Moleküle außerdem in ihrer Wirkung auf lebende Organismen, den sogenannten physiologischen Eigenschaften.
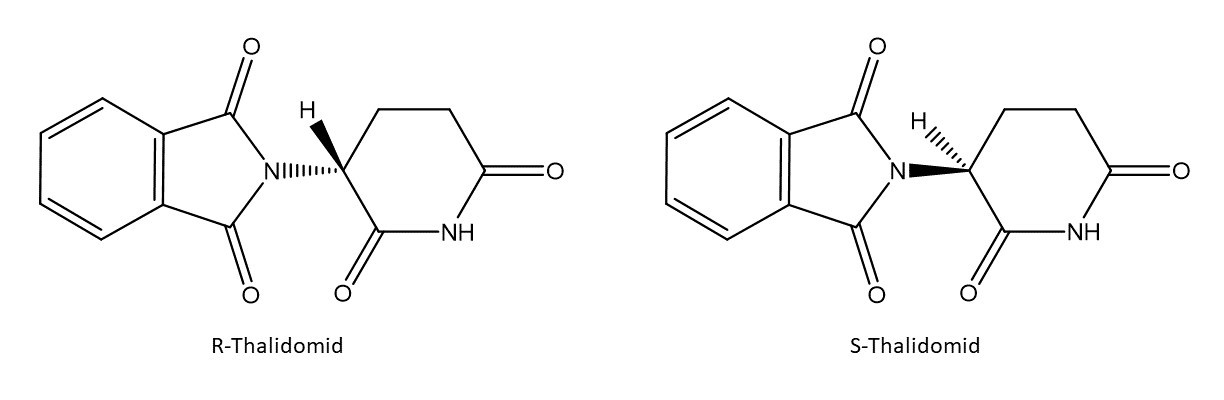
Ein bekanntes Beispiel dafür ist der Contergan-Skandal aus dem Jahr 1961. Hier kam heraus, dass eine Version des chiralen Medikamentes (R-Thalidomid) ein gutes Schlafmittel ist, während die andere Version (S-Thalidomid) zu schwerwiegenden Behinderungen in Kindern führte.