Mit der Standard-Wasserstoffelektrode als Bezugspunkt lassen sich für viele Elemente die Standardpotenziale ermitteln. Die Standardpotenziale der Elemente bilden eine elektrochemische Spannungsreihe.
Einige Elemente der elektrochemischen Spannungsreihe siehst du in der folgenden Tabelle (Abb. 1):
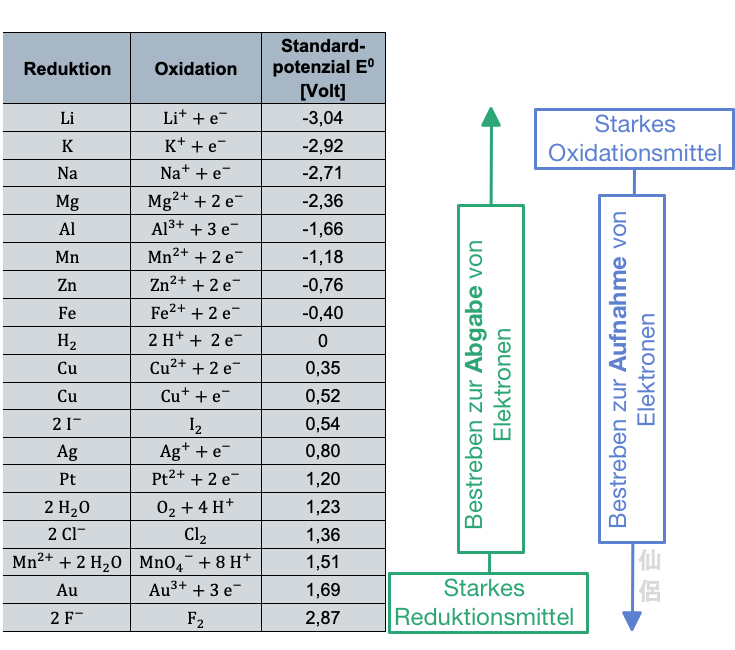
Abb 1. Die elektrochemische Spannungsreihe, eigenes Werk, CC BY Sien-Lie Saleh
Mithilfe des Standardpotenzials lässt sich die Richtung von Redoxreaktionen vorhersagen: Das stärkere Oxidationsmittel reagiert mit dem stärkeren Reduktionsmittel, weil dadurch der größte Energiegewinn erzielt wird.
Die Spannung U einer galvanischen Zelle berechnet man aus der Differenz der Standardpotenziale. Sie heißt auch Potenzialdifferenz:
oder alternativ:
Du hast noch nicht genug vom Thema?
Hier findest du noch weitere passende Inhalte zum Thema:
