1 Übersicht
Inhalt des Kurses
In diesem Kurs lernst du wichtige Grundbaustoffe von Zellen kennen.
Vorkenntnisse
Du solltest schon über einige chemische Grundkenntnisse (Atome, Molekül, chemische Bindungen) verfügen.
Kursdauer
~5 Minuten
2 Einführung
Jede Zelle besteht aus einer Vielzahl chemischer Verbindungen. Jeder dieser Stoffe ist für die Funktionsweise der Zelle notwendig und erfüllt bestimmte Aufgaben. Wenn das Element Kohlenstoff in den Verbindungen vorkommt, spricht man von organischen Verbindungen. Einige organische Verbindungen wie Kohlenhydrate oder Proteine kommen besonders häufig in Zellen vor.
Die Stoffe werden ständig in den Zellen auf- und abgebaut beziehungsweise zwischen den Zellen ausgetauscht.

Abb.1: Molekulare Verbindungen sind wichtige Bestandteile von Zellen
3 Kohlenhydrate
Kohlenhydrate sind wichtige Energieträger und Strukturgeber von Lebewesen. Die kleinste Einheit sind Einfachzucker (Monosaccaride). Diese können von Disaccariden (Zweifachzucker) bis zu großen Polysaccariden bestehend aus mehreren Tausend Monosaccariden zusammengeschlossen sein.
Aufbau von Einfachzucker
Entsprechend ihrer Anzahl an Kohlenstoffatomen im Molekül unterteilt man die Monosaccaride in Hexosen (sechs C-Atome) und Pentosen (fünf C-Atome). Wichtigster Vertreter der Hexosen ist Glucose (Traubenzucker). Seine Summenformel lautet .
Weitere wichtige Hexosen sind Fructose und Galaktose, der Grundbaustein von Milchzucker. Bedeutende Pentosen sind Ribose und Desoxyribose, wichtige Bestandteile der Ribonukleinsäure (RNA) beziehungsweise der DNA.
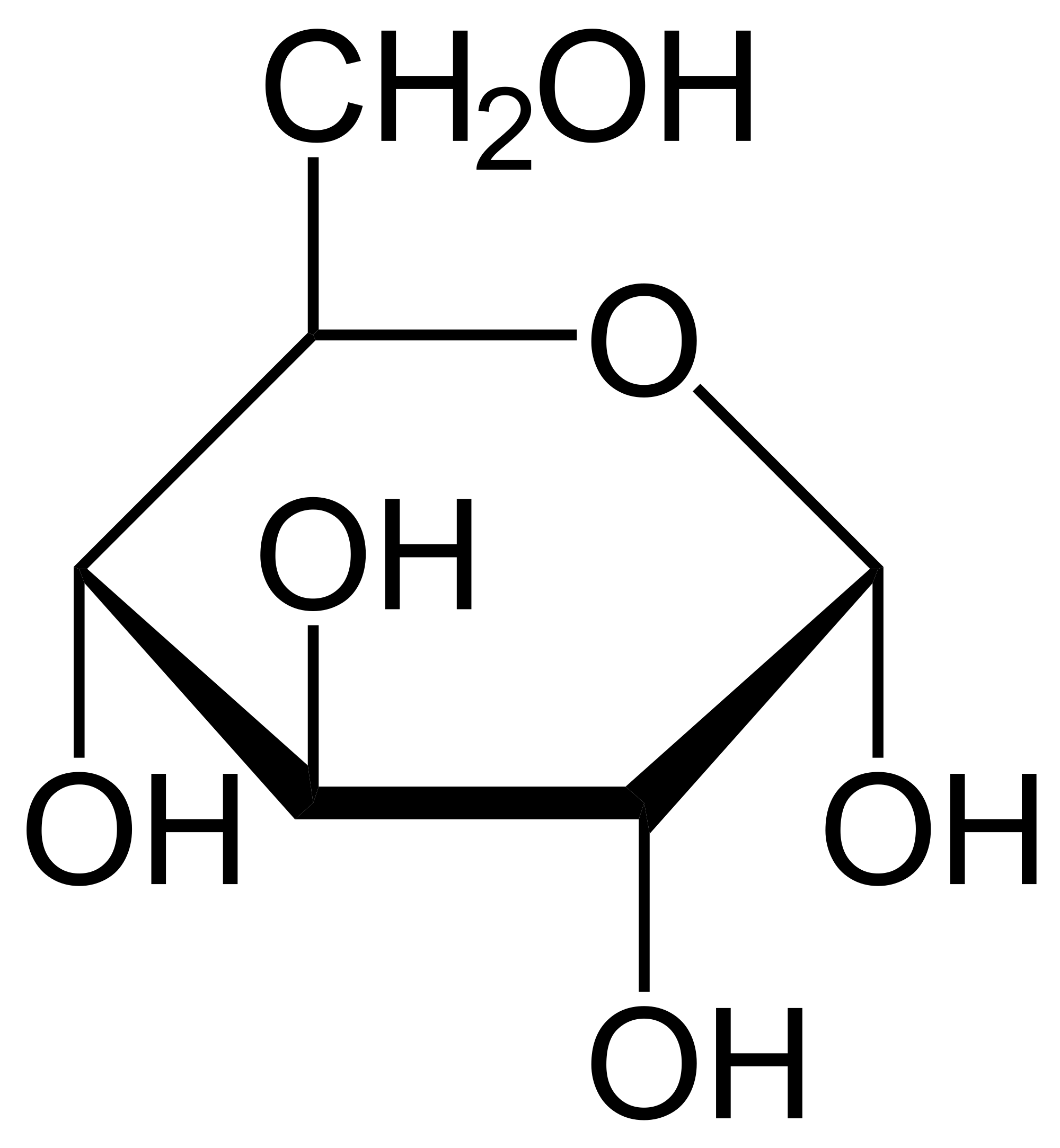
Abb.2: Glucosemolekül
Aufbau von Mehrfachzucker
Mehrfachzucker (Polysaccaride) setzen sich aus vielen Monosaccariden (Einfachzuckern) zusammen. Die kleinsten Mehrfachzucker sind sogenannte Disaccaride, die aus der Reaktion zweier Monosaccaride unter Wasserabspaltung entstehen. Die entstehende Bindung nennt man glykosidische Bindung. Die bekanntesten Zweifachzucker sind Laktose (zwei Galaktose-Moleküle) und Maltose (zwei Glucosemoleküle).
Große Polysaccaride bestehen aus bis zu mehreren Tausend Monosaccariden. Typische Vertreter sind Stärke und Cellulose. Sie dienen als Reservestoffe beziehungsweise Gerüstsubstanz.

Abb.3: Laktose ist auch als Milchzucker bekannt.
4 Lipide
Zu den Lipiden gehören chemisch sehr verschiedene Stoffe. Sie haben die gemeinsame Eigenschaft, dass sie in unpolaren Lösungsmitteln gut löslich sind, sich in polaren Lösungsmitteln wie Wasser allerdings nicht lösen.
Fette
Fette bestehen aus dem Alkohol Glycerin, der unter Wasserabspaltung mit drei meist verschiedenen Fettsäuren reagiert. Sie werden deshalb auch Triglyceride genannt. Fette sind eine energiereiche Speichersubstanz.
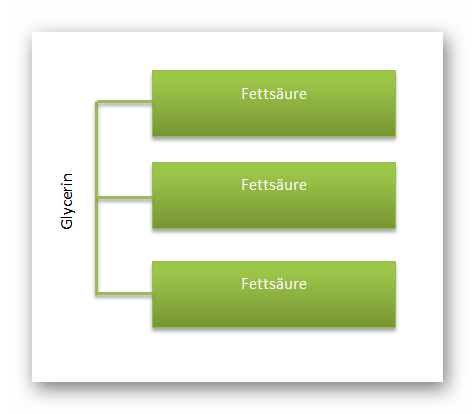
Abb.4: Allgemeiner Aufbau von Fetten
Phospholipide
Phospholipide sind wichtige Bausteine der Biomembran. Sie bestehen aus einem polaren, hydrophilen Molekülabschnitt, der in Wasser löslich ist, sowie zwei unpolaren, hydrophoben Fettsäuren. Ein Beispiel für ein Phospholipid ist Lecithin.
5 Proteine
Funktionen
Proteine erfüllen im Organismus eine Vielzahl wichtiger Funktionen:
Katalyse chemischer Reaktionen (Enzyme, z.B. Amylase)
Bewegung (z.B. Aktin-, Myosinfilamente)
Gerüstsubstanz (z.B. Kreatin)
Transport (z.B. Hämoglobin)
Immunität (Antikörper)
Nährstoffe (z.B. Hühnereiweiß)
Grundbestandteil Aminosäuren
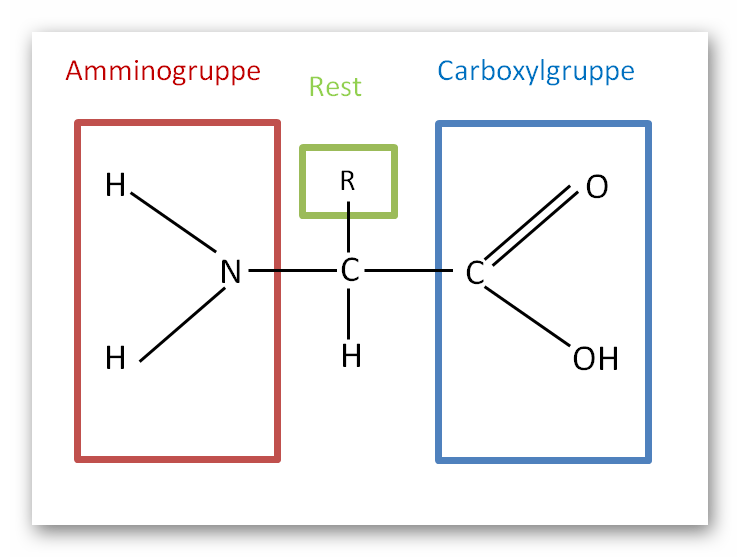
Proteine bestehen aus Aminosäuren. Alle 20 existierenden Aminosäuren sind immer nach dem gleichen Grundbauplan aufgebaut: An ein zentrales Kohlenstoffatom knüpfen ein Wasserstoffatom, die Aminogruppe (), die Carboxylgruppe () sowie ein organischer Rest (R). Die verschiedenen Aminosäuren unterscheiden sich lediglich im Aufbau des organischen Restes.
Abb.5: Aufbau von Aminosäuren
Struktur von Proteinen
Zwei Aminosäuren können sich über eine Peptitbindung zum Dipeptid verknüpfen. Dabei reagiert die - Gruppe der Carboxylgruppe einer Aminosäure mit dem - Atom der Aminogruppe einer anderen Aminosäure. Werden viele Aminosäuren über Peptidbindungen miteinander verknüpft, so spricht man von einem Polypeptid. Ab etwa 100 Aminosäuren werden diese Polypeptide Proteine genannt.
Die Vielfalt der Proteine entsteht lediglich durch den unterschiedlichen Rest der Aminosäuren sowie deren kettenartige Abfolge. Diese Aminosäuresequenz wird als Primärstruktur bezeichnet. Sie kann auch die räumliche Struktur des Proteins mitbeeinflussen und ist so entscheidend für die Funktion eines Proteins.
Die Sekundärstruktur ist die dreidimensionale Anordnung der Polypeptidketten durch Wasserstoffbrückenbindungen zwischen bestimmten Aminosäuren. Dabei gibt es nur zwei mögliche Anordnungen: Die - Helix-Struktur oder die Faltblattstruktur.
Abb.6: Strukturebenen von Proteinen
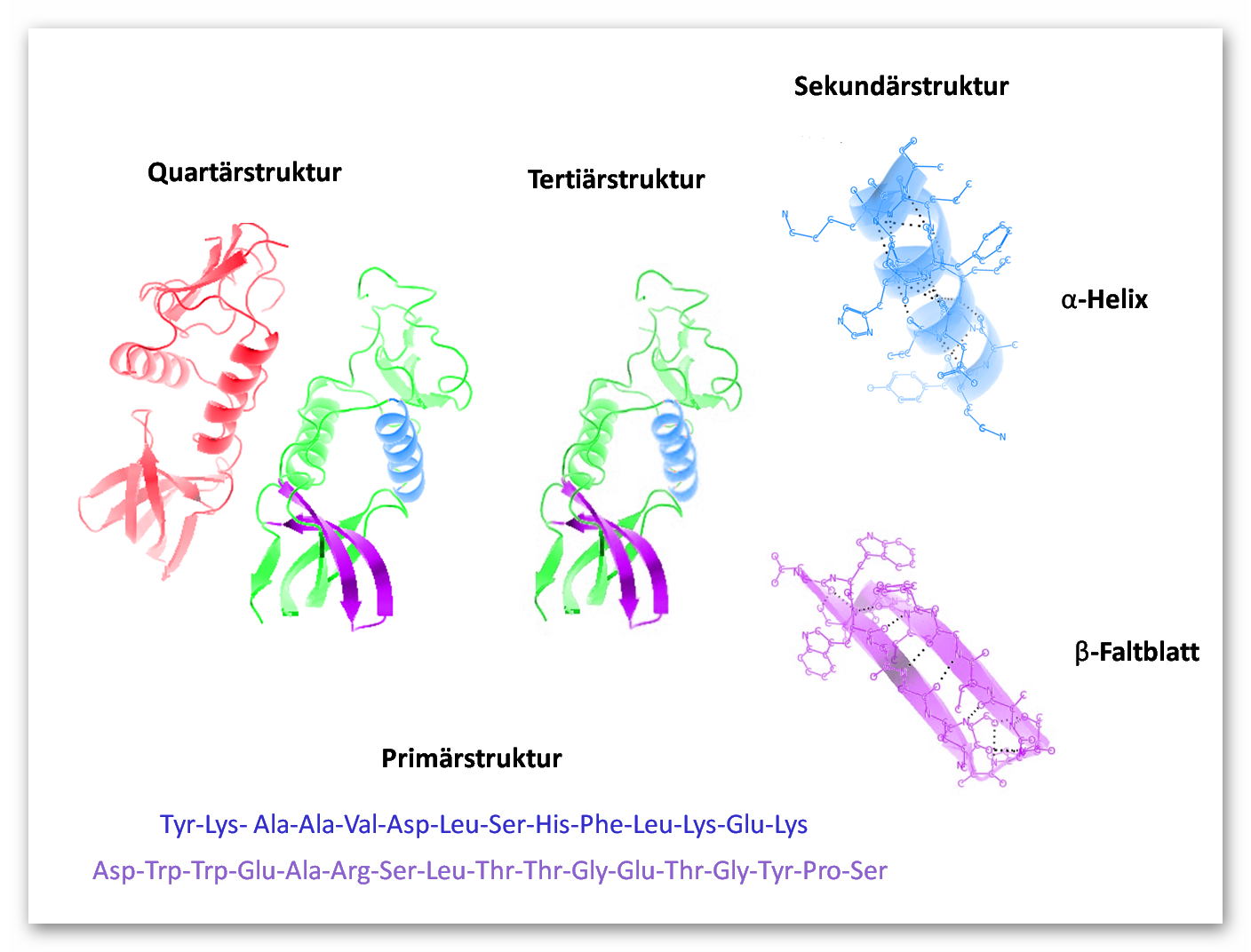
Die Tertiärstruktur eines Proteins entsteht durch erneutes Verbinden der Polypeptidkette in der Sekundärstruktur. Die Bindungen erfolgen zwischen den Resten der Aminosäuren über verschiedene chemische Bindungen, wie Wasserstoffbrückenbindungen oder Elektronenpaarbindungen.
Einige Proteine setzen sich aus mehreren Polypeptidketten zusammen. Diese Anordnung bezeichnet man als Quatärstruktur. Die einzelnen Ketten werden Untereinheiten genannt.
6 Aufgaben
Laden
