Anorganische Salze sind Atomverbindungen bestehend aus Metallen und Nichtmetallen, Salze bestehen aus einem Kation (positiv geladenes Atom) und einem Anion (negativ geladenes Atom), die in einer ionischen Verbindung vorliegen. Sie kommen in kristalliner Form vor und können sich sehr gut in Wasser lösen. Die Atome sind untereinander in einem Atomgitter verknüpft.
Salze kommen sehr oft in Gesteinen vor.

Aufbau
Die Struktur der Salze ist sehr stabil und kompakt. Dabei sind Kationen und Anionen in einem Gitter angeordnet und halten durch die starke elektromagnetische Beziehung gut zusammen. Das Gitter nennt man auch Ionengitter.
Struktur von NaCl in Ionengitterform
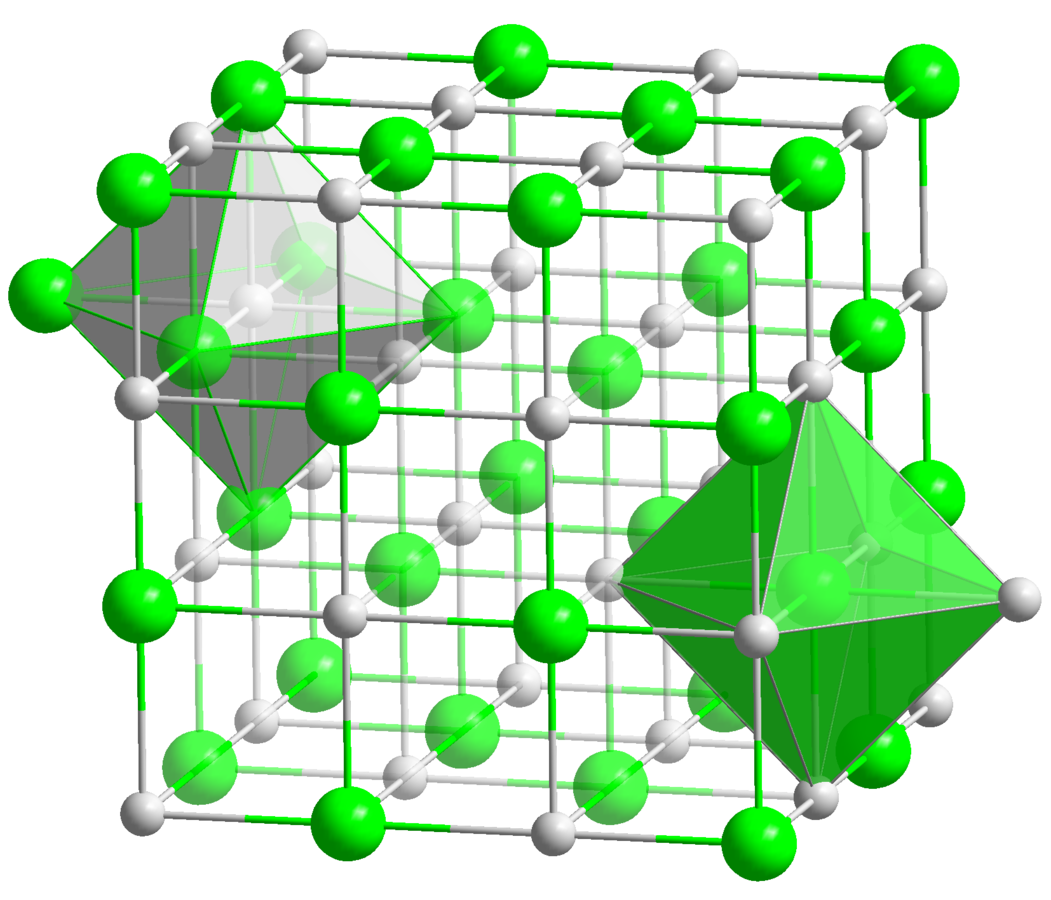
Eigenschaften der Salze
Salze sind in ihrer kristallinen Form nicht leitend, wirken also wie Isolatoren. Das liegt daran, dass die Ladungsträger (in diesem Fall Ionen) fest in der Gitterstruktur sitzen und sich nicht bewegen können.
Löst man Salz in Wasser oder schmilzt man es unter hohen Temperaturen, dann kann Salz sehr gut leiten. Denn hier sind die Ionen (Ladungsträger) frei beweglich.
Salze haben einen sehr hohen Schmelzpunkt. Da die Verbindung sehr stark ist, wird sehr viel Energie benötigt, um sie zu brechen.
Salze sind sehr gut wasserlöslich. Die Ionen im Ionengitter können sehr gut mit Wasser-Molekülen, die Dipol-Dipol-Wechselwirkungen besitzen, reagieren.
Salze sind aber dafür unlöslich in unpolaren Lösungsmitteln wie Benzin oder Öl. Das liegt daran, dass die unpolaren Moleküle des Lösungsmittels schlecht mit den Ionen des Ionengitters reagiert.
Salze sind spröde und haben glatte Bruchkanten.
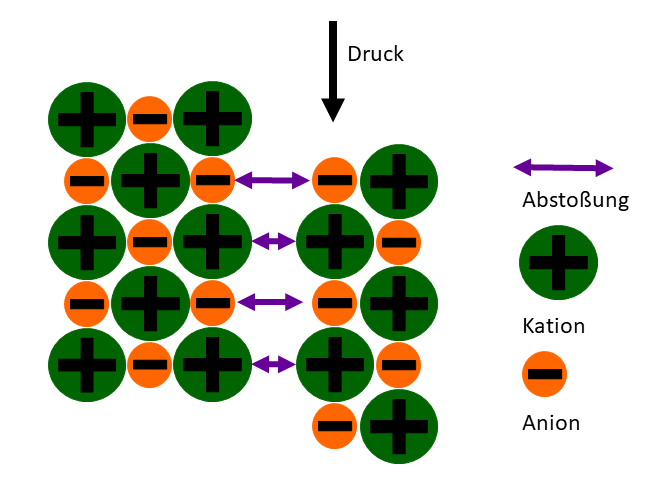
Wieso sind Salze spröde?
Die einzelnen Kat- und Anionen sind in einem Ionengitter verbunden. Die Kationen (grün) und die Anionen (orange) sind abwechselnd aneinandergereiht, so ziehen sie sich gegenseitig an. Sobald eine mechanische Kraft ausgeübt wird, verschiebt sich ein Teil dieses Gitters. So treffen Anionen aufeinander, und Kationen auf Kationen, das führt zu einer starken Abstoßung.
Dadurch wird der ganze Teil des Gitters abgestoßen. So kommt es zu einer glatten Bruchkante.