1 Einführung: Stoffe in unserer Umwelt
Wir sind überall von Stoffen umgeben. In der Luft ist Sauerstoff, den jedes Lebewesen zum Atmen benötigt. Wasser verwenden wir zum Waschen, Kochen und Trinken. Papier finden wir als Informationsmedium in Zeitungen, Büchern oder Schulheften oder auch als Reinigungsmaterial bei Zellstoff-Taschentuch und Klopapier.
Durch die Allgegenwärtigkeit ist es notwendig, Stoffe und ihre Eigenschaften zu erkennen, zu verstehen und vorherzubestimmen. Dieser Kurs wird sich insbesondere damit beschäftigen, wie wir Stoffe beschreiben können und auf Grundlage verschiedener Beschreibungen Stoffe unterscheiden können.

Auch Nahrungsmittel sind eine wichtige Gruppe von Stoffen!
2 Übung: Stoffe in unserer Umwelt
Du kennst bestimmt auch viele Stoffe. Nehme dir 10 Minuten Zeit und finde möglichst viele verschiedene Stoffe. Hast du schon ein Gefühlt dafür, wo man eher von einer "Substanz" sprechen wird oder wo man eher eine der anderen Formulierungen "Naturprodukt", "Rohstoff", … verwenden wird?
Du wirst sicherlich feststellen, dass es sich hier nicht um klar definierte, gegeneinander abgegrenzte Begriffe handelt. Vielmehr kann je nach Sachverhalt ein oder mehrere Begriffe benutzt werden.
3 Definition und Beispiele
Definition und alternative Begriffe
Der Begriff des Stoffes geht einher mit dem Vorhandensein einer Masse ("Materie"). Die Begriffe Materie und Stoff können equivalent verwendet werden, d.h. jede Materie ist zwangsläufig ein Stoff und andersherum. Der Begriff "Stoff" impliziert hierbei tendenziell den Fokus auf Verwendungseigenschaften, während der Begriff "Materie" eine deutlich fundamental-physikalischere Sichtweise impliziert.Es gibt viele weitere Begriffe, die in diesem Zusammenhang synonym (d.h. gleichbedeutend) verwendet werden, z.B.
Substanz
Rohprodukt, Naturprodukt, Endprodukt, Produkt
Rohstoff, Naturstoff, Werkstoff, …
Mit der Benutzung alternativer Begriff wird gleichzeitig oft ein bestimmter Ursprung oder eine bestimmte Verwendung des Stoffes ausgedrückt. Hierbei wird aber auch der sehr allgemeine Begriff "Stoff" eingeschränkt, der ja zunächst allumfassend ist. Der Begriff "Substanz" erscheint häufig im Zusammenhang mit offensichtlich chemisch oder physikalisch aktiven Stoffen, z.B. in einem Chemielabor, bei einem Schülerversuch oder in einem Medikament, insbesondere wenn ein wissenschaftlicher Stoffname verwendet wird, wie eine chemische Formel.
Beispiele
Du hast bereits im ersten Absatz einige wenige Beispiele für Stoffe und ihre Verwendung kennengelernt. Hier sollen insbesondere zu den verschiedenen kennengelernten Begrifflichkeiten Beispiele genannt werden.
Stoff | Substanz | Rohstoff | Werkstoff | Naturprodukt |
|---|---|---|---|---|
Ethanol | x | x | ||
Wasser | x | x | ||
Eisen | x | x | x | |
"Holz" | x | x |
Nicht-Beispiele: Wir haben gesehen, dass fast alles in unserer Welt ein Stoff ist. Dennoch gibt es Dinge, die explizit kein Stoff ist. Dies liegt insbesondere an dem Fehlen der vorher besprochenen Materie-Eigenschaft.
Licht, auch elektromagnetische Strahlung im Allgemeinen wie Ultraviolett, Röntgen, Radiowellen, Radar
Schall, d.h. Geräusche und Töne, aber auch Ultraschall
Wärme, nicht nur Wärmestrahlung (siehe "Licht"), sondern auch als Wärmeleitung
4 Was sind (Stoff-)Eigenschaften?
Es gibt also eine Vielzahl von verschiedenen Stoffen, die in ganz verschiedenen Zusammenhängen zum Einsatz kommen. Wir wollen nicht nur passiv diesen Stoffen und ihrer Auswirkung auf uns ausgesetzt sein, sondern auch aktiv über die Auswahl und Veränderung von Stoffen unsere Umwelt verändern. Ein wesentlicher Schritt zu einer aktiven Beeinflussung ist das Identifizieren verschiedener Eigenschaften von Stoffen.
Bedeutung von Eigenschaften
Das Erkennen und die Zuweisung von Eigenschaften von Stoffen ist die Beschreibung anhand von Merkmalen. Insbesondere ermöglicht die Zuweisung von Eigenschaften eine Abgrenzung von anderen Stoffen, die andere Merkmale aufweisen. Dort wo eine Eigenschaft quantitativ bestimmbar ist (d.h. messbar), spricht man auch von einer Größe. Es gibt aber auch Eigenschaften, wie z.B. Farbe, die nicht quantifizierbar sind.
Die Eigenschaft der Messbarkeit bezieht sich auf die Möglichkeit, ein Maß oder auch Vergleichsmaß anzulegen und durch Vergleich mit dem Maß einen Wert zu bestimmen. Zum Beispiel kann eine Länge gemessen werden, indem mit einem Lineal ("Metermaß") verglichen wird. Zum Beispiel kann ein Gewicht bestimmt werden, indem auf einer Balkenwaage mit einem bekannten Gewicht verglichen wird.
Es gibt zwei verschiedene Arten von messbaren Eigenschaften
extensive Größen, die sich durch direkte Messung, d.h. Vergleich, ermitteln lassen, sich aber zusammen mit der Probengröße ändern
intensive Größen, die sich erst durch In-Beziehung-Setzen von direkt messbaren Eigenschaften ergeben, sich dafür aber nicht mehr mit der Probengröße ändern.
In einem späteren eigenen Abschnitt werden wir genauer auf diese zwei Arten und ihre Unterscheidung eingehen.
Es gibt es aber auch qualitative (also nicht-messbare) Eigenschaften, wie z.B. Farbe, Form, Geschmack, Aggregatzustand. Diese lassen sich nicht in obiges Schema aus messbaren Eigenschaften einordnen.
Zu konkreten Beispielen und Unterscheidung/Merkmalen wird später noch viel mehr erklärt. Dies soll nur einen kurzen Einblick geben.
5 Übung: Stoffeigenschaften
Laden
6 Darstellung von messbaren Eigenschaften
Um eine quantifizierbare (d.h messbare) Größe anzugeben, wird eine bestimmte Schreibweise verwendet. Um später Missverständnisse und Fehler zu vermeiden, ist es wichtig, sich immer an diese Form zu halten.
Die Größe und die Einheit wird häufig durch Symbole abgekürzt. Dies führt zu einer verbesserten Übersichtlichkeit. Der "Mal-Punkt" zwischen Wert und Einheit ist formal eine Multiplikation, der Operator wird aber häufig weggelassen. Weil die Darstellung formal eine (mathematische) Gleichung ist, kann sie auch zu folgender Form umgestellt werden. Diese Form findet sich häufig in Tabellenwerken, um die wiederholte Angabe der Einheit bei unterschiedlichen Werten zu umgehen.
Häufig werden gleiche oder ähnliche Symbole für bestimmte Größen verwendet, z.B. für das Volumen. Dennoch ist die Verwendung nicht einheitlich. In jedem Dokument muss definiert werden, welche Größen durch welches Symbol ausgedrückt werden.
Dagegen ist die Verwendung von Symbolen für die Einheit klar geregelt, z.B. steht das immer für die Maßeinheit "Liter". Die Einheiten leiten sich grundsätzlich von den SI-Basiseinheiten ab. Hier ist die Einheit für das Volumen , die über den Umrechnungsfaktor von "Kubik-Meter" in "Liter" umgerechnet werden kann.
7 Übung: Darstellung von messbaren Eigenschaften
8 Extensive und intensive Größen
In einem früheren Abschnitt wurde bereits erwähnt, dass es zwei verschiedene Arten von Größen gibt. Diese sollen hier genauer vorgestellt und erklärt werden.
Extensive Größen
Extensive Größen zeichnen sich dadurch aus, dass sie (also der gemessene Wert) sich mit der Größe der untersuchten Stoffportion ändern. Die Änderung findet oft sogar im selben Maß, man sagt "direkt proportional", statt. Wichtige extensive Größen sind
Anzahl
Volumen, d.h. der Rauminhalt
Fläche
Länge
Masse
Stoffmenge
…
Die Masse eines Stoffes ändert sich also mit dessen Anzahl. Gibt es mehr von einem Stoff, so ist er schwerer, gibt es weniger, wird er leichter.
Insbesondere die zuletzt genannte "Stoffmenge" hat eine sehr zentrale Bedeutung in der Chemie. Es handelt sich hier um einen klar definierten Ausdruck! Die Stoffmenge ist so wichtig, dass sie eine der 7 vorgenannten SI-Basiseinheiten ist.
Intensive Größen
Intensive Größen zeichnen sich dadurch aus, dass sie (also der gemessene Wert) sich nicht mit der Größe der untersuchten Stoffportion ändern. Das bedeutet gleichzeitig, dass insbesondere die intensiven Größen verwendet werden können, um eine vorhandene (unbekannte) Stoffart zu identifizieren oder zu charakterisieren. Einige bekannte intensive Größen sind
Dichte
Konzentration
…
Die Dichte ist definiert als Verhältnis von Masse zu Volumen einer bestimmten Stoffportion. Bei Vergrößerung der Stoffportion ändert sich die Masse im gleichen Maße wie das Volumen. Dadurch bleibt die Dichte konstant für den verwendeten Stoff.
Bei Betrachtung des obigen Rechenbeispiels wird zusätzlich ein anderer Zusammenhang deutlich. Wir hatten eine intensive Größe berechnet, aber dafür zwei extensive Größen und in Bezug zueinander gesetzt. Genau genommen haben wir (und das ist wichtig!) eine extensive Größe durch eine andere geteilt. Hieraus lässt sich ein allgemein gültiger Ansatz entwickeln.
9 Übung: Extensive und intensive Stoffeigenschaften
Laden
10 Klassifizierung von Stoffen
Wir haben bisher gelernt, dass…
es viele verschiedene Stoffe gibt
die Stoffe anhand ihrer Eigenschaften identifiziert und unterschieden werden können
es verschiedene Typen von Eigenschaften gibt, anhand derer wir verschieden aussagekräftige Merkmale finden können.
Weil es eine große Vielfalt von Stoffen gibt, wird es sinnvoll sein, eine grobe Struktur dafür zu entwickeln. Innerhalb dieser Struktur werden Stoffe eingruppiert. Die folgende Grafik greift auf viele Konzepte voraus, die du erst in späteren Abschnitten oder gar anderen Kursen kennenlernst. Dennoch solltest du ein grundsätzliches Gefühl dafür entwickeln, dass es nicht nur eine Sorte Stoff, sondern eher viele verschiedene Stofftypen gibt.
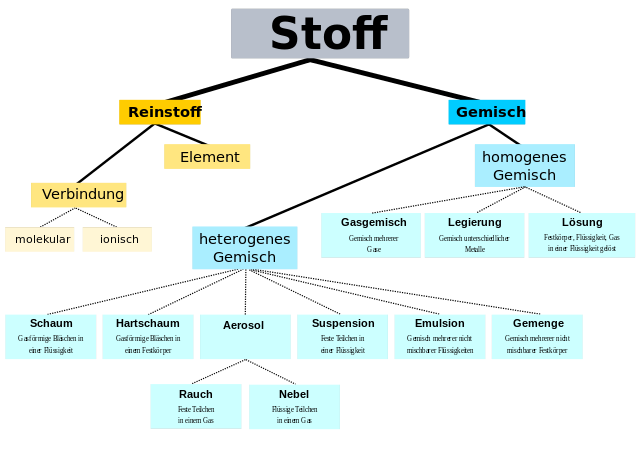
Quelle: Peter Krimbacher, CC BY-SA 2.0 DE, Wikimedia commons
11 Übersicht
Inhalt des Kurses
In diesem Kurs werden verschiedene Stoffe betrachtet, sowie deren Eigenschaften.
Außerdem geht der Kurs auf Messbarkeit von Eigenschaften ein.
Zielgruppe
Das Thema "Stoffe und Stoffeigenschaften" ist meist zu Beginn der Chemie in der Schule angesiedelt. Dieser Kurs richtet sich dennoch eher an ein fortgeschrittenes Publikum.
