RedOx-Reaktionen spielen in der Chemie eine wichtige Rolle, so sind sie die Basis für viele Stoffwechsel- und Verbrennungsvorgänge, technische Produktionsprozesse und Nachweisreaktionen und sie können sogar zum Verschweißen von Gleisen verwendet werden.

RedOx-Reaktion ist die Abkürzung für eine Reduktions-Oxidations-Reaktion.
Bei diesen Reaktionen handelt es sich um chemische Reaktionen.
RedOx-Reaktionen sind definiert als Reaktionen mit Elektronenübertragung.
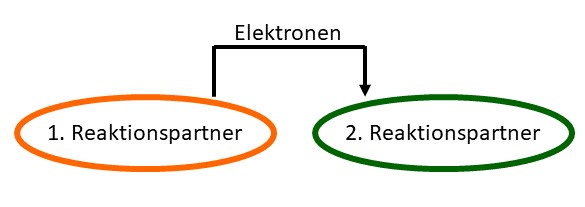
Bei einer Redoxreaktion werden Elektronen des einen Reaktionspartners auf einen anderen Reaktionspartner übertragen. Dazu gibt ein Stoff ein Teil seiner Elektronen ab, während ein anderer Stoff diese Elektronen aufnimmt.
Die Abgabe von Elektronen wird als Oxidation bezeichnet. Allgemeingültig formuliert ist die Erhöhung der Oxidationszahl eine Oxidation.
Die Aufnahme von Elektronen wird als Reduktion bezeichnet. Allgemeingültig formuliert ist die Erniedrigung der Oxidationszahl eine Reduktion.
Ein Stoff, der in der RedOx-Reaktion selber Elektronen abgibt, wird durch den jeweils anderen Stoff oxidiert.
Ein Stoff, der in der RedOx-Reaktion selber Elektronen aufnimmt, wird durch den jeweils anderen Stoff reduziert.
Als Reduktionsmittel werden Reaktionspartner bezeichent, die zur Reduktion "anregen" und Elektronen abgeben. Sie werden oxidiert.
Als Oxidationsmittel werden Reaktionspartner bezeichnet, die zur Oxidation "anregen" und Elektronen aufnehmen. Sie werden reduziert.
In einem Satz: Das Reduktionsmittel wird bei einer RedOx-Reaktion oxidiert, während das Oxidationsmittel bei einer RedOx-Reaktion reduziert wird.
Du hast noch nicht genug vom Thema?
Hier findest du noch weitere passende Inhalte zum Thema:
Artikel
Quellen
- https://de.wikipedia.org/wiki/Thermitreaktion
- https://de.wikipedia.org/wiki/Redoxreaktion
- Abb.1: Skatebiker, Wikimedia
